How Can We Help?
Transport et Pollution
- Introduction
- Sources
- Contamination de l’eau
- Contamination de l’air
- Contamination des sédiments
- Études de cas
Transport et Pollution
Le relargage massif de PFAS dans l’environnement ainsi que leur grande persistance explique l’ubiquité de ces composés dans les milieux naturels. Aussi, les PFAS regroupent un grand nombre de substances, provenant de sources variables et ayant des propriétés diverses. Par conséquent, leur comportement peut varier en fonction de leur identité (famille, sous famille, isomère, ect.) mais aussi en fonction des propriétés de chaque milieu..
La majeure partie des émission est rejetée dans l’eau (de l’ordre de 90%), le reste est libéré dans l’atmosphère. Ainsi, les plus gros réservoirs de PFAS de l’environnement sont les océans et les sédiments1.
Sources
Directes et indirectes
Les PFAS sont relâchés dans l’environnement lors de leur fabrication, de l’utilisation des produits manufacturés et lors de leur mise en décharge. On distingue alors les sources2 :
- directes : lorsque le contaminant est libéré lors du cycle de vie du produit ou dans les rejets industriels
- indirectes : lorsqu’ils sont issus de la dégradation de précurseurs.
Les PFAS issus de sources indirectes sont les plus difficiles à quantifier. En effet, leur origine est inconnue et leur transport suit une dynamique complexe. Les précurseurs ont été décrits comme la source principale des PFAAs (e.g. PFOA, PFOS, PFNA, PFBA, PFHxS, ect.). 3
Ponctuelles et diffuses
Comme abordé précédemment, les PFAS peuvent être issus de sources directes mais aussi de la dégradation de leurs précurseurs. Ils se transforment en substances persistantes et bioaccumulables qui sont libérées vers le sol, les eaux de surface et souterraines. Les sites majeurs de pollutions sont des sources ponctuelles4,5 telles que :
- les STEP où ont lieu des processus de dégradation des précurseurs (retrouvés dans les effluents et les boues d’épuration)
- les sites d’entraînement aux incendies, à proximité des aéroports ou des bases militaires, où l’utilisation d’AFFF libère des PFAS dans le sol, les aquifères et les eaux de surface
- usines de fabrication
- les décharges où sont entreposés des produits plus ou moins riches en PFAS

Il existe également des sources de pollution diffuses6 dont :
-
les retombées atmosphériques sèches et humides (particules en suspension dans l’air générées par les sources ponctuelles)
-
les fuites et ruissellements depuis les rues et/ou les sites contaminés par l’épandage de bio-solides ou suite aux retombées atmosphériques
Contamination de l’eau
La grande solubilité et faible volatilité de certains PFAS font que les milieux aqueux stockent une grande partie des composés relâchés dans l’environnement. Néanmoins, comme dans le cas des aérosols, l’eau peut également être source de PFAS.
Eau potable
D’après une étude d’échelle mondiale réalisée par Kaboré et al. (2018)7, les PFOA et PFOS sont encore (malgré leur bannissement en Occident) les PFAS dominants dans l’eau du robinet. On y trouve également des FASAs tels que le FBSA et le FHxSA mais aussi des short-chains PFSAs tels que le PFEtS, le PFPrS, le PFPeS et le PFHpS.
Les échantillons d’eau en bouteille étudiés par Kaboré et al. (2018) contiennent principalement du FPBA, PFBS, PFOA et du PFHxS. Les concentrations en PFAS dans l’eau en bouteilles sont moins importantes que celles trouvées dans l’eau du robinet (<1.6ng/L).
Coggan et al. (2019)8 ont analysés l’eau potable de Melbourne pour 53 PFAS. Les seules substances détectées sont résumées dans le tableau ci-dessous.
| PFAS | PFBA | PFHxA | PFOA | PFHxS | PFOS | 6:2 FtS |
| Gammes de concentration en ng/L | <0.59-0.79 | <0.87-1.2 | 0.58-1.8 | <0.69 | <0.8 | <0.56-4.3 |
Eaux de surface
Coggan et al. (2019)9, ont réalisé une série d’ananlyse sur plusieurs eaux de surface en amont et en aval d’un ancien site d’entraînement aux incendie en Australie. Ils ont étudié la présence de 53 PFAS. Les concentrations des substances détectées sont iniquées dans le tableau ci-dessous.
| Concentrations (ng/L)
Rivière amont |
Concentrations (ng/L)
Zone humide aval |
Concentrations (ng/L)
Lac aval |
|
| PFBA | 2,2 | 31 | 2,5 |
| PFPeA | ND | 30 | – |
| PFHxA | 2,3 | 186 | 2,1 |
| PFHpA | – | 12 | – |
| PFOA | 3,3 | 8,4 | 2,5 |
| PFBS | – | 21 | 1,0 |
| PFPeS | – | 26 | – |
| PFHxS | 0,95 | 193 | 3,4 |
| PFHpS | – | 5,4 | – |
| PFOS | 2,9 | 137 | 4,3 |
| 6:2FTS | 9,1 | 8,7 | 3,1 |
Océan
Ahrens et al. (2010)10, ont conduit une étude sur deux profils verticaux dans la baie de Tokyo. Ils ont mesuré les taux de PFAS dans l’eau (contentant 97% des PFAS) et dans les matières en suspensions (abritant 3% des PFAS).
Dans la phase dissoute, ont été retrouvés des PFSAs (C6 et C8), du FOSA, du EtFOSAA mais aussi des PFCAs (C4 à C11). Le PFBA (C4 PFCA) est le composé retrouvé en majeure quantité (52%). La somme des concentrations en PFAS dans la colonne d’eau varie entre 16,7 et 42,3 ng/L.
Dans la phase de matière en suspension du PFHxS, du PFOS, du PFOSA et des PFCAS (C7 à C11) ont été identifiés. La somme de concentration de PFAS dans les matières en suspensions est comprise entre 6,4 et 15,1ng/g (poids sec). Le composé prédominant est le PFOS (représente 48% des PFAS). Les concentrations de PFAS dans les matières en suspensions étaient 30 à 40 fois supérieures à celles observées dans les sédiments.
Cette étude a montré que les PFSAs, les FASAs et les long-chains PFCAs ont un fort potentiel d’intéraction avec la matière en suspension des milieux aqueux. Ce phénomène peut alors conduire à l’emprisonnement des polluant lors de la sédimentation. Les PFCAs ayant une chaîne perfluorée contenant plus de onze carbone ont été retrouvés uniquement dans les sédiments.
Contamination de l’air
Les PFAS contenus dans l’atmosphère proviennent :
- des rejets atmosphériques des manufactures et des décharges11,
- de la dégradation des précurseurs volatiles : les PFAS volatiles (FTOHs, FASAs, FASEs,..), une fois dans l’atmosphère peuvent être dégradés durant l’oxydation atmosphérique et forment des composés intermédiaires ou se transforment en PFAAs12,
- des embruns marins : les PFAAs sont majoritairement présents dans les océans sous leur forme anionique soluble et peu volatile. Une partie de ces PFAAs est conduite vers l’air via les embruns marins. Une partie des PFAAs contenus dans l’air retombe vers les terres, perpétuant ainsi la contamination en PFAAs. L’efficacité de ce phénomène varie évidemment en fonction des propriétés de chaque molécules13,14.
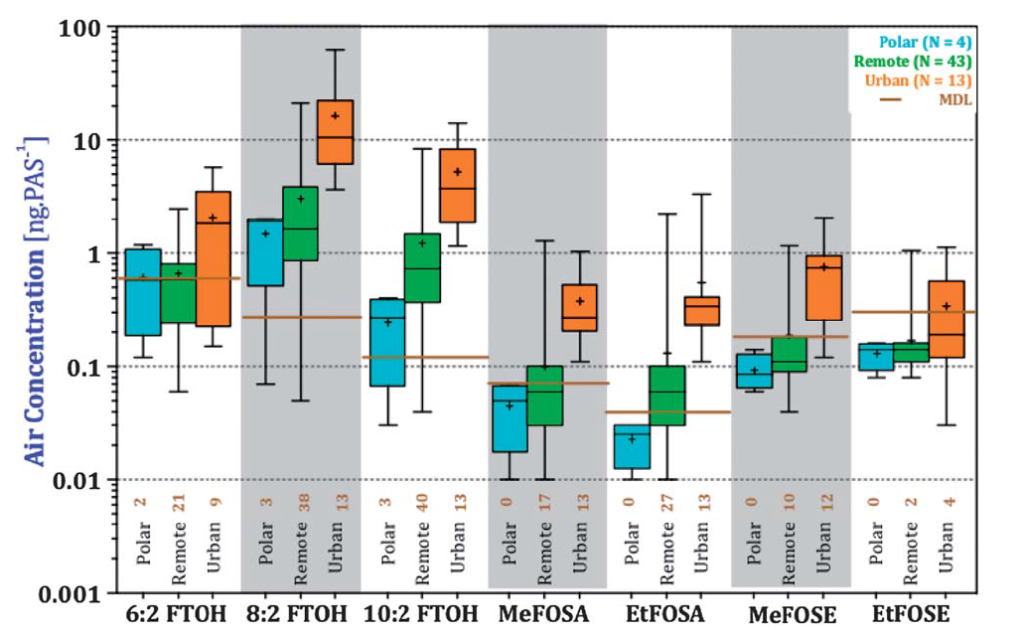
Gawor et al. (2014)15 ont mesurés les concentrations de nPFAS (e.g. FTOHs, FASAs, FASEs, N-FASAs..) dans l’air à différents endroits du globe (sur les 6 continents) pendant 6 ans (2006-2012). La quantité moyenne de nPFAS dans l’air est résumée par le graphique ci-dessous.
|
|
Contamination des sédiments
Higgins et al. (2005) 17, ont étudié la présence de PFAS dans des sédiments de la baie de San Fransico et dans des boues d’épuration. Pour accéder à leurs résultats cliquez ici.
Études de cas
En décharge
Les rejets de PFAS liés aux décharges ont été étudiés par Hamid et al. (2018)18, ce paragraphe résume leur conclusions.
Différents produits mis en décharge peuvent contenir des PFAS. Parmi eux se trouvent :
- les bio-solides (boues d’épuration, ect.),
- les papiers, tissus et tapis
- les matériaux de constructions
- les composés électroniques
Les PFAS sont libérés depuis les déchets jusqu’à la décharge par un processus de lixiviation biotique et abiotique (e.g. désorption). Aussi, une partie des PFAS, solubles sous leur forme anionique (e.g. PFAAs), se mélange avec les lixivats tandis que les PFAS plus volatils (avec une faible solubilité et une haute pression vapeur) (e.g. FTOHs) se répandent dans l’atmosphère si ils ne sont pas captés par le système de récupération de gaz de la décharge.
Lixiviats
Les lixiviats des centres d’enfouissement étanches ou provenant des décharges aménagées sont envoyés vers les centrales de traitement des eaux (STEP). Celles-ci doivent traiter des eaux déjà chargées en PFAS et ne sont actuellement pas équipées pour traiter efficacement ce type de molécules.
De nombreux PFAS ont été retrouvés dans les lixiviats de plusieurs décharges, notamment :
- des PFAAs, dont la somme des concentration varie entre 0.1 et 10µg/L et provenant des déchets et de la dégradation des précurseurs. Les PFCAs sont les substances dominantes dans les lixiviats. Les PFAAs contenus dans les lixiviats sont majoritairement des short-chains depuis le bannissement des long-chains.
- des fluorotélomères (e.g. n:2 FTCAs, n:2 FTUCAs, n:2 FTSAs, n:3 FTCAs) dont certains sont issus de la dégradation des FTOHs
- les dérivés de sulfonamides : FASAAs (e.g. EtFOSAA et N-FASAs (e.g. EtFOSE)
- des PAPs très vite dégradés en PFCAs et FTCAs
Rejets atmosphériques
Les décharges sont des sources non négligeables de PFAS dans l’atmosphère. En effet, la concentration dans l’air mesurée au niveau des décharges est 2 à 30 fois supérieur aux points de référence (à priori non contaminés par les PFAS). Aussi l’air ambiant des décharges contient :
- 90% de FTOHs avec 50 à 65 % de 8:2 FTOH et 40 % de 6:2 FTOH
- des sulfonamides et dérivés : FOSA, N-FOSAs, FOSEs
- des PFAAs, détectés dans les phases gazeuse et particulaire, dont du PFBA, PFHxA et du PFOA (majoritaire)
Très peu de PFOS est détecté dans l’air sûrement à cause de la sorbtion de cette substance par les déchets solides et l’efficacité du système de récupération de gaz de la décharge.
Contamination d’une nappe exposée aux AFFFs et aux rejets de STEP
Weber et al. (2017)19 ont réalisé une étude sur la contamination aux PFAS d’une nappe libre. Ce site est d’une part soumis une pollution provenant d’un ancien site d’entraînement militaire dédié aux incendies. D’autre part, l’aquifère est situé sous d’anciens lits d’infiltration d’effluents de STEP riches en PFAS (cf. Figure 1). Il s’agit de deux sources de PFAS à long terme. En effet, les concentrations au droit de ces sites sont élevées malgré leur fermeture depuis 1985 et 1995 respectivement.
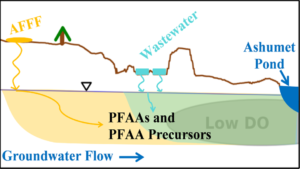
Le site d’entraînement militaire est la source majoritaire de PFAS. Il libère surtout des PFAAs et des FtS (en particulier du PFOS, du PFOA et du 6:2 FtS). Les lits d’infiltrations constituent également une source de PFAS mais en moindre quantité. Les eaux usées sont surtout chargées en PFOA et PFNA.
Le rejet des eaux usées ayant cessé en 1995, la persistance de concentrations élevées en PFAS à proximité du site d’épandage suggère que les PFAS sont absorbés dans les sédiments et sont lentement libérés et transportés jusqu’à la nappe. Les substances piégées dans la zone non-saturée pourraient subir des dégradations et se transformer en PFAS plus mobiles, atteignant plus facilement la nappe. Le même phénomène peut être observé au droit du site d’entraînement aux incendies. 18 à 20 ans après l’arrêt des émissions, la zone non-saturée fournit toujours des PFAS. Une estimation de la vitesse de migration du PFOS a été réalisée. D’après Weber et al. (2017), il faudrait entre 3 et 30 ans au PFOS pour traverser 17m de zone non-saturée, soit 0,57 à 5,7m/an et 15 ans pour parcourir 780m dans la nappe, soit 52m/an.
- Ahrens, L. and Bundschuh, M. (2014). Fate and effects of poly- and perfluoroalkyl substances in the aquatic environment: A review. Environmental Toxicology and Chemistry, 2014, 33, 1921-1929.
- Buck, R. C. et al. (2011). Perfluoroalkyl and Polyfluoroalkyl Substances in the Environment : Terminology, Classification, and Origins. Integrated Environmental Assessment and Management, 2011, 7, 513-541.
- Liu, J. and Avendaño, S. M. (2013).. Environment International, 2013, 61, 98 – 114 Microbial degradation of polyfluoroalkyl chemicals in the environment : A review.
- Ahrens, L. and Bundschuh, M. (2014). Fate and effects of poly- and perfluoroalkyl substances in the aquatic environment: A review. Environmental Toxicology and Chemistry, 2014, 33, 1921-1929.
- Kaboré, H. A. et al. (2018). Worldwide drinking water occurrence and levels of newly-identified perfluoroalkyl and polyfluoroalkyl substances. Science of The Total Environment, 2018, 616-617, 1089-1100.
- Ahrens, L. and Bundschuh, M. (2014). Fate and effects of poly- and perfluoroalkyl substances in the aquatic environment: A review.Environmental Toxicology and Chemistry, 2014, 33, 1921-1929.
- Kaboré, H. A. et al. (2018). Worldwide drinking water occurrence and levels of newly-identified perfluoroalkyl and polyfluoroalkyl substances.Science of The Total Environment, 2018, 616-617, 1089-1100.
- Coggan, T. L. et al. (2019). A single analytical method for the determination of 53 legacy and emerging per- and polyfluoroalkyl substances (PFAS) in aqueous matrices. Analytical and Bioanalytical Chemistry, 2019
- Coggan, T. L. et al. (2019). A single analytical method for the determination of 53 legacy and emerging per- and polyfluoroalkyl substances (PFAS) in aqueous matrices. Analytical and Bioanalytical Chemistry, 2019
- Ahrens, L. et al. (2010). Distribution of polyfluoroalkyl compounds in water, suspended particulate matter and sediment from Tokyo Bay, Japan. Chemosphere, 2010, 79, 266 – 272.
- Hamid, H.; Li, L. Y. and Grace, J. R. (2018). Review of the fate and transformation of per- and polyfluoroalkyl substances (PFASs) in landfills. Environmental Pollution, 2018, 235, 74-84.
- Ahrens, L. and Bundschuh, M. (2014). Fate and effects of poly- and perfluoroalkyl substances in the aquatic environment: A review.Environmental Toxicology and Chemistry, 2014, 33, 1921-1929.
- Johansson, J. H. et al. (2019). Global transport of perfluoroalkyl acids via sea spray aerosol. Environ. Sci.: Processes Impacts, 2019, 21, 635-649.
- McMurdo, C. J. et al. (2008). Aerosol Enrichment of the Surfactant PFO and Mediation of the Water−Air Transport of Gaseous PFOA. Environmental Science & Technology, 2008, 42, 3969-3974.
- Gawor, A. et al. (2014). Neutral polyfluoroalkyl substances in the global Atmosphere. Environ. Sci.: Processes Impacts, 2014, 16, 404-413.
- Ellis, D. A. et al. (2004). Degradation of Fluorotelomer Alcohols: A Likely Atmospheric Source of Perfluorinated Carboxylic Acids. Environmental Science & Technology, 2004, 38, 3316-3321.
- Higgins, C. P. et al. (2005). Quantitative Determination of Perfluorochemicals in Sediments and Domestic Sludge. Environmental Science & Technology, 2005, 39, 3946-3956
- Hamid, H.; Li, L. Y. and Grace, J. R. (2018). Review of the fate and transformation of per- and polyfluoroalkyl substances (PFASs) in landfills. Environmental Pollution, 2018, 235, 74-84.
- Weber, A. K. et al. (2017). Geochemical and Hydrologic Factors Controlling Subsurface Transport of Poly- and Perfluoroalkyl Substances, Cape Cod, Massachusetts. Environmental Science & Technology, 2017, 51, 4269-4279.


